PARASITOSIS INTESTINAL Y/O VISCERAL
INTRODUCCIÓN
Las infecciones parasitarias
intestinales provocan un número no despreciable de niños infestados en nuestro
país.
La patología producida por este tipo
de parásitos ya conocida en nuestro medio (como giardiasis, oxiuriasis,
ascariosis…), hay que añadir un incremento en el número de casos y nuevos tipos
de parasitación por patógenos menos frecuentes hasta ahora, pero que se están
incrementando paralelamente a la nueva situación sociodemográfica de nuestro
país: aumento de niños procedentes de áreas endémicas por inmigración
internacional, como lo es el caso del vecino país colombiano, que llegan
desplazados a consecuencia de la situación política que enfrenta ese país.
Es, por tanto, necesario para los
médicos un conocimiento epidemiológico, microbiológico y clínico adaptado a
esta situación y disponer de las opciones de diagnóstico y terapéutica para el
correcto manejo de estas personas.
DEFINICIÓN Y CLASIFICACIÓN
Las parasitosis intestinales son
infecciones intestinales que pueden producirse
por la ingestión de quistes de
protozoos, huevos o larvas de gusanos o por la penetración de larvas por vía
transcutánea desde el suelo. Cada uno de ellos va
a realizar un recorrido específico en
el huésped y afectará a uno o varios órganos, con lo que las podemos clasificar
según el tipo de parásito y la afectación que provoquen en los distintos
órganos y sistemas (Tabla I). Sólo nos vamos a referir a los que infestan niños
con mayor frecuencia y que tienen una repercusión directa en el aparato
digestivo, ya que otros parásitos con predominio tisular se tratan en otros
temas de esta monografía.
TABLA I.
Clasificación
de las principales parasitosis intestinales
|
Protozoos
|
1. Afectación exclusivamente
digestiva: Giardiasis: Giardia lamblia
2. Afectación digestiva y
potencialmente en tejidos:
a. Amebiasis: Entamoeba
histolytica/dispar
b. Criptosporidiasis: Cryptosporidium
|
Helmintos
|
1. Nemathelmintos o nematodos o
gusanos cilíndricos:
a. Afectación exclusivamente
digestiva:
– Oxiuriasis: Enterobius
vermicularis
– Tricocefalosis: Trichuris
trichiura
b. Afectación digestiva y pulmonar:
– Ascariosis: Ascaris
lumbricoides
– Anquilostomiasis o uncinariasis:
- Ancylostoma duodenale
- Necator americanus
c. Afectación cutánea, digestiva y
pulmonar:
– Estrongiloidiasis: Strongyloides
stercoralis
2. Plathelmintos o cestodos o
gusanos planos
a. Afectación exclusivamente
digestiva:
– Himenolepiasis: Hymenolepis
nana
– Teniasis: Taenia saginata y
solium
b. Posibilidad de afectación
digestiva y potencialmente en tejidos:
–
Teniasis: Taenia solium: Cisticercosis
|
GIARDIASIS
(Giardia intestinalis: G. lamblia y G. duodenalis)
Se trata de la parasitosis intestinal
más frecuente a nivel mundial, con distribución universal. Tras la ingesta de
quistes del protozoo, éstos dan lugar a trofozoítos en el intestino delgado
(ID) que permanecen fijados a la mucosa hasta que se produce su bipartición, en
la que se forman quistes que caen a la luz intestinal y son eliminados con las
heces. Los quistes son muy infectantes y pueden permanecer viables por largos
períodos de tiempo en suelos y aguas hasta que vuelven a ser ingeridos mediante
alimentos contaminados.
La sintomatología puede ser muy variada:
a) asintomático: más frecuente en niños de áreas endémicas; b) giardiasis aguda:
diarrea acuosa que puede cambiar sus características a esteatorreicas, deposiciones
muy fétidas, distensión abdominal con dolor y pérdida de peso; y c) giardiasis
crónica: sintomatología subaguda y asocia signos de malabsorción, desnutrición y
anemia.
Diagnóstico
Determinación de quistes en materia fecal o de trofozoítos en el cuadro agudo con deposiciones acuosas. Es
importante recoger muestras seriadas en días alternos, pues la eliminación es
irregular y aumenta la rentabilidad diagnóstica. En el caso de pacientes que
presentan sintomatología persistente y estudio de heces negativo se recomienda
realización de ELISA en heces.
(véase tabla II)
El porcentaje de resistencia de
Giardia a metronidazol está aumentando, por lo que es necesario conocer
alternativas eficaces. Es importante extremar las medidas que controlen la
contaminación fecal de aguas, así como la ingesta de alimentos y bebidas en
condiciones dudosas en viajes a zonas endémicas.
(Entamoeba histolytica/dispar)
Tras la ingestión de quistes
contenidos en alimentos y aguas contaminadas o por déficit de higiene en manos,
los trofozoítos eclosionan en la luz intestinal y colónica, y pueden permanecer
en ese lugar o invadir la pared intestinal para formar nuevos quistes tras
bipartición, que son eliminados al exterior por la materia fecal y volver a
contaminar agua, tierra y alimentos. En el proceso de invasión de la mucosa y
submucosa intestinal, producen ulceraciones responsables de parte de la
sintomatología de la amebiasis, así como la posibilidad de diseminación a
distancia y afectación de otros órganos diana (absceso hepático).
Muy variada, desde formas
asintomáticas hasta cuadros fulminantes:
a. Amebiasis asintomática: representa
el 90% del total.
b. Amebiasis intestinal invasora aguda
o colitis amebiana disentérica: gran número de deposiciones con contenido mucoso
y hemático, tenesmo franco, con volumen de la deposición muy abundante en un
principio y casi inexistente posteriormente, dolor abdominal importante, tipo
cólico. En casos de pacientes desnutridos o inmunodeprimidos pueden presentarse
casos de colitis amebiana fulminante, perforación y formación de amebomas con cuadros
de obstrucción intestinal asociados.
c. Amebiasis intestinal invasora
crónica o colitis amebiana no disentérica: dolor abdominal tipo cólico con
cambio del ritmo intestinal, intercalando periodos de estreñimiento con
deposiciones diarreicas, tenesmo leve, sensación de plenitud posprandial,
náuseas, distensión abdominal, meteorismo y borborigmos.
Diagnóstico
Mediante visualización de quistes en materia
fecal o de trofozoítos en cuadro agudo con deposiciones acuosas. Para diferenciar
E. histolytica, ameba patógena, de E. dispar, ameba no patógena
que no precisa tratamiento, es necesario una PCR-RT, prueba que solo puede
realizarse en algunos en centros especializados.
Tratamiento y prevención
(véase tabla II)
El portador asintomático tiene un papel
fundamental en la perpetuación de la endemia; la amebiasis intestinal tiene, además,
tendencia familiar y predominio en grupos hacinados, por lo que resulta fundamental
extremar las medidas de higiene personal y comunitarias.
CRIPTOSPORIDIASIS
(Cryptosporidium)
Son coccidios protozoarios con distribución
universal que pueden producir infección en animales y humanos. Se produce por
ingesta de oocitos procedentes de alimentos y aguas contaminados (piscinas comunitarias,
parques acuáticos, aguas de lagos y pantanos…) o por vía fecal-oral (frecuente
en guarderías). Tras la ingesta de oocitos en alimentos o aguas contaminados,
se liberan esporozoítos con capacidad de unirse a los bordes en cepillo de las
células epiteliales intestinales, en donde pueden reproducirse asexual o sexualmente
(esta última mediante formación de micro y macro-gametos, su unión y la
formación de nuevos oocitos) para ser eliminados posteriormente junto a la
materia fecal y perpetuar la posibilidad de infección.
Clínica
Muy variada.
a) Asintomática;
b) forma intestinal: cuadro de
deposiciones diarreicas acuosas con dolor abdominal, fiebre, náuseas, vómitos y
signos de deshidratación y pérdida de peso, autolimitado y frecuente en niños
en epidemias relacionadas con guarderías o piscinas. Puede ser más prolongado
en pacientes con inmunodepresión;
c) forma extraintestinal: en
inmunodeprimidos (SIDA) con afectación de sistema respiratorio, hepatitis,
artritis reactivas y afectación ocular.
Mediante visualización de oocitos en materia
fecal. También se utiliza frecuentemente técnicas de EIA en muestra fecal con
alta sensibilidad y especificidad.
Tratamiento y prevención
Medidas de soporte: reposición de líquidos
y electrolitos y, en casos graves, fluidoterapia intravenosa y/o terapias nutricionales.
En pacientes inmunodeprimidos se asocia tratamiento antibiótico (véase tabla
II). En pacientes con SIDA, la terapia antirretroviral consigue mejoría en el
estatus inmune y acortar la sintomatología.
Es fundamental incrementar las medidas
de higiene para evitar la transmisión fecal-oral y limitar el uso de piscinas en
pacientes con diarrea.
OXIURIASIS
(Enterobius vermicularis)
La hembra del parásito se desplaza hasta
zona perianal, principalmente con horario nocturno, donde deposita sus huevos, muy
infectantes, que quedan adheridos a la piel o en la ropa. Con el rascado de la
zona, se establecen bajo las uñas y se perpetúa la autoinfección por
transmisión fecal-oral.
Clínica
Mucho más habitual en niños que en adultos,
frecuentemente asintomática. Síntomas por acción mecánica (prurito o sensación de
cuerpo extraño), invasión genital (vulvovaginitis), despertares nocturnos, sobreinfección
secundaria a excoriaciones por rascado, dolor abdominal que en ocasiones puede
ser recurrente, localizarse en FID y simular apendicitis aguda.
No está demostrada su relación con
síntomas que tradicionalmente se relacionan con oxiuriasis como bruxismo,
enuresis nocturna o prurito nasal.
• Test de Graham: uso de cinta
adhesiva transparente por la mañana antes de defecación o lavado. Visualiza los huevos depositados por la hembra en zona
perianal.
• Visualización directa del gusano adulto
en la exploración anal o vaginal.
Tratamiento y prevención
(véase tabla II)
Los huevos son muy resistentes si
persiste adecuado nivel de humedad, por lo que puede permanecer largo tiempo en
la ropa. Es necesario extremar las medidas de higiene de inodoros, manos y uñas
y lavar con agua caliente y lejía la ropa de cama, pijamas y toallas. Es
necesario el tratamiento de todos los miembros de la familia ante la
posibilidad de perpetuación de la infección.
TRICOCEFALOSIS
(Trichuris trichiura)
Geohelmintiasis producida por la ingesta
de huevos embrionados procedente de alimentos, tierra (típico en niños) o aguas
contaminadas. Las larvas maduran en ciego y colon ascendente, donde permanecen enclavados
a la mucosa, produciendo lesión mecánica y traumática con inflamación local, y
desde donde vuelvan a producir nuevos huevos fértiles que son eliminados por
materia fecal.
Clínica
Depende del grado de parasitación: desde
asintomática, pasando por dolor cólico y deposiciones diarreicas ocasionales, hasta
cuadros disenteriformes con deposiciones muco-sanguinolentas (en pacientes inmunodeprimidos)
y prolapso rectal.
Identificación de huevos en materia fecal.
En casos graves, plantear el diagnóstico diferencial con amebiasis, disentería bacilar
y colitis ulcerosa.
Tratamiento y prevención (véase tabla II)
Extremar medidas de higiene personal, adecuada
eliminación de excretas, utilización de agua potable y correcto lavado de alimentos.
Vigilancia de los juegos con arena de niños en parques, lavar manos.
(Ascaris lumbricoides)
Es la helmintiasis más frecuente y con
mayor distribución a nivel mundial. Tras ingestión de material contaminado, las
larvas eclosionan en ID, atraviesan la pared intestinal, se incorporan al
sistema portal y llegan nivel pulmonar, donde penetran en los alveolos y
ascienden hasta vías respiratorias altas que por la tos y deglución, llegan de
nuevo a ID, donde se transforman en adultos, producen nuevos huevos, que se
eliminan por material fecal.
• Digestiva: dolor abdominal difuso
(por irritación mecánica) y menos frecuentemente meteorismo, vómitos y diarrea.
• Respiratorio: desde sintomatología inespecífica
hasta síndrome de Löeffler (cuadro respiratorio agudo con fiebre de varios
días, tos y expectoración abundantes y signos de condensación pulmonar
transitoria, consecuencia delpaso pulmonar de las larvas y una
respuesta de hipersensibilidad asociada).
• Otras: anorexia, malnutrición,
obstrucción intestinal, absceso hepático.
Diagnóstico
Hallazgo del parásito o sus huevos en materia
fecal o de las larvas en esputo o material gástrico si coincide con fase
pulmonar.
Tratamiento y prevención (ver tabla II)
ANQUILOSTOMIASIS O UNCINARIASIS
(Ancylostoma duodenale y Necator
americanus)
Los huevos de estos dos helmintos se eliminan
por materia fecal y eclosionan en un terreno favorecedor dando lugar a un tipo
de larva que precisa una nueva modificación para obtener capacidad infectante
mediante penetración por la piel
(en A. duodenale también puede
provocar infección por ingestión vía oral). Una vez atravesada la piel, se
dirigen al sistema venoso o linfático para llegar a sistema cardiaco derecho y
circulación pulmonar, penetrar en los alveolos, madurar allí y ascender por
vías respiratorias
altas para ser deglutidas y alcanzar duodeno y yeyuno, donde se fijan y comienzan a producir nuevos huevos fecundados. Al fijarse en ID, los gusanos adultos causan una lesión mecánica que provoca pérdida sanguínea progresiva y crónica.
altas para ser deglutidas y alcanzar duodeno y yeyuno, donde se fijan y comienzan a producir nuevos huevos fecundados. Al fijarse en ID, los gusanos adultos causan una lesión mecánica que provoca pérdida sanguínea progresiva y crónica.
Clínica
• Piel: “síndrome de Larva Migrans Cutánea”:
dermatitis pruriginosa, transitoria y recurrente en pies y zonas interdigitales,
donde penetran y se desplazan hasta alcanzar el sistema circulatorio.
• Respiratoria: desde síntomas
inespecíficos a síndrome de Löeffler (ver ascariosis).
• Síndrome anémico.
Diagnóstico
Hallazgo de huevos del parásito en materia
fecal. Clínico: área endémica + síntomas cutáneos y pulmonares + anemia +
contacto con tierra.
Tratamiento y prevención (véase tabla II)
Al tratamiento etiológico hay que
añadir el de la anemia, que puede llegar a ser muy severa. Alas medidas de tipo
preventivo habituales (uso de letrinas y zapatos, saneamiento ambiental y
educación poblacional) se unen actualmente tratamiento comunitario en zonas de
alta endemia.
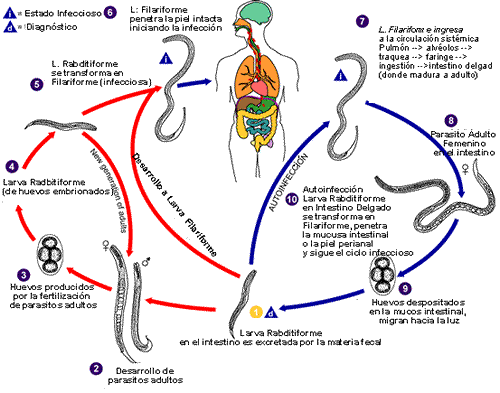
ESTRONGILOIDIASIS
(Strongyloides stercoralis)
Esta geohelmintiasis presenta un ciclo
vital con distintas posibilidades:
a. Ciclo directo: la larva, que se
encuentra en el suelo, se modifica para poder penetrar a través de la piel al
sistema circulatorio, donde llega a sistema cardiaco derecho y circulación
pulmonar, asciende por las vías respiratorias hasta ser deglutida y dirigirse a
la mucosa del ID. Allí se transforma en hembra infectante, produce nuevos
huevos que eclosionan y se dirigen a la luz intestinal, desde donde son
eliminados al exterior.
b. Ciclo indirecto: incluye una o
varias generaciones de larvas en vida libre (sin afectación humana), hasta que
se produce la modificación que hace a la larva infectante para el hombre.
c. Ciclo de autoinfección: la
modificación larvaria se produce en la luz intestinal
en lugar del exterior y posteriormente
penetra en el sistema circulatorio y realiza un recorrido similar al del ciclo
directo. Es lo que se denomina síndrome de hiperinfección por S. stercoralis,y
explica que pueda existir una parasitosis persistente sin necesidad de
reinfecciones externas, así como la afectación de otros órganos: hígado, pulmón,
SNC, sistema ganglionar…
Clínica
En general depende del estado
inmunitario del paciente.
• Piel: “síndrome de Larva Currens”: dermatitis
pruriginosa por el paso tanscutáneo de la larva y el recorrido realizado hasta
llegar a circulación sistémica.
• Respiratorio: suele provocar
sintomatología menor como tos y expectoración, pero también se han descrito casos
de neumonitis y síndrome de Löeffler.
• Digestiva: la intensidad de la
sintomatología está en relación con el grado de parasitosis: dolor epigástrico,
vómitos, anorexia, períodos de diarrea que se alternan con estreñimiento.
• Síndrome de hiperinfestación: casi exclusivo
del paciente inmunocomprometido.
Los síntomas anteriormente señalados
se expresan con mayor severidad.
Diagnóstico
Eosinofilia importante, más evidentesi
la extracción coincide con el paso pulmonar del parásito. La visualización del parásito
en material fecal es diagnóstica pero difícil por la irregularidad en la
eliminación, al encontrarse a nivel de mucosa-submucosa intestinal. Necesita
microbiólogo experto. Serología mediante EIA, sensibilidad > 90% pero
reactividad cruzada con filarias y otros nematodos.
Tratamiento y prevención
(véase tabla II)
Debe ser siempre tratada ante la
posibilidad de autoinfección y la curación debe ser comprobada
parasitológicamente. Son importantes las medidas preventivas de tipo individual
y general: uso de letrinas y zapatos, saneamiento ambiental, educación poblacional.
HIMENOLEPIASIS
(Hymenolepis nana)
El hombre puede ser tanto huésped intermedio
como definitivo para la parasitación por este cestodo de pequeño tamaño.
Los huevos son ya infectantes al salir
por la materia fecal y son ingeridos mediante prácticas de escasa higiene. Los huevos
alcanzan el duodeno, donde se adhieren a la mucosa intestinal y penetran en la
mucosa, obteniendo la forma de cisticercoide.
Posteriormente podrá pasar de nuevo a
la luz intestinal y formar el parásito adulto con capacidad productora de huevos.
Síntomas digestivos, generalmente leves,
como dolor abdominal, meteorismo, diarrea y bajo peso si la infección se cronifica.
Diagnóstico
Eosinofilia si está circulante, lo
habitual es que curse sin eosinofilia. Visualización de huevos en materia
fecal. El número de ellos encontrado está directamente relacionado con el grado
de
parasitación.
parasitación.
Tratamiento y prevención
(véase tabla II)
En general es una tenia más resistente
por la presencia de cisticercoides, en la mucosa intestinal, por lo que el
ciclo de tratamiento debe ser repetido entre 7-10
TENIASIS
(Taenia saginata)
El ser humano puede actuar con este parásito
como huésped intermediario o definitivo. El paciente parasitado elimina proglótides
y huevos en la materia fecal, que son ingeridos por animales (cerdo en T.
solium y ganado vacuno en T. saginata), en los que se forman
cisticercos en músculo estriado que son posteriormente ingeridos por el hombre
mediante carnes poco o mal cocinadas. Una vez en el Intestino Delgado, el
parásito se adhiere a la pared, crece y comienza a producir de nuevo
proglótides y huevos. La mayoría son infecciones únicas, producidas por una
tenia solamente.
Es escasa, principalmente de tipo
irritativa mecánica, e inespecífica: meteorismo, náuseas, dolor abdominal, etc.
Puede ocurrir la salida de proglótides a nivel anal con molestia y prurito
perineal, así como la observación del deslizamiento de las mismas por los MMII
dejando un líquido lechoso muy pruriginoso y muy rico en huevos.
Diagnóstico
Mediante la observación por parte del paciente
de salida de proglótides en heces. Visualización de proglótides en materia
fecal. Determinación de coproantígenos por EIA (aunque presenta reactividad cruzada
con otros cestodos), útil para la comprobación de la efectividad del
tratamiento.
Tratamiento y prevención
(véase tabla II)
La prevención debe ser realizada mediante
un adecuado control de seguridad de las carnes en los mataderos, así como con
una adecuada cocción o congelación
prolongada de las carnes. La adecuada eliminación
de las excretas resulta también fundamental. Criterios de curación: hallazgo
del escólex en materia fecal tras tratamiento; examen de heces negativo durante
3 meses siguientes a tratamiento o negativización de coproantígenos.
CISTICERCOSIS
(Taenia solium)
Es la afectación tisular de la larva
de la T. solium. El hombre ingiere huevos de este subtipo de tenia y al
llegar a Intestino Delgado, penetran la pared hasta alcanzar el sistema circulatorio,
el pulmón y posteriormente el corazón izquierdo desde donde son distribuidos
por la circulación arterial a distintos lugares del organismo (más frecuentemente
Sistema Nerviso Central, tejido celular subcutáneo, músculo y ojo), en los que
forma los denominados quistes o cisticercos, que pueden permanecer durante años
y que, al morir, producen una importante reacción inmunológica e inflamatoria que
provoca gran parte de la sintomatología.
• Neurocisticercosis: epilepsia de
aparición tardía, cefalea y signos de Hipertensión Endocraneal, síndrome
psicótico, meningitis aséptica, síndrome de los pares craneales, síndrome
medular.
• Nódulos subcutáneos y musculares blandos
y no dolorosos, generalmente asociados a la neurocisticercosis.
• Afectación oftálmica: generalmente única
y unilateral. Si la larva muere, puede producir importante reacción inflamatoria
y provocar importante reacción uveal, desprendimiento de retina y ceguera.
Diagnóstico
Imagen: Tomografía Computarizada
cerebral o Resonancia Magnetica en paciente procedente de área endémica con inicio
de sintomatología neurológica descrita.
Inmunodiagnóstico con Inmunoblot posee
mayor sensibilidad y especificidad que el diagnóstico por EIA.
Tratamiento y prevención
(véase tabla II)
Puede ser necesario añadir al
tratamiento, corticoides, antiepilépticos e incluso cirugía si aparecen signos
de HTIC. Es necesario realizar control de imagen 3-6 meses después de concluir
el tratamiento.
Para la prevención es fundamental
realizar una correcta cocción de la carne de cerdo así como extremar las
medidas de higiene en la cría de éstos.
|
TABLA II.
TRATAMIENTO DE
LOS PARÁSITOS INTESTINALES MÁS FRECUENTES
|
|||||
|
PATÓGENO
|
FÁRMACO
|
DOSIS
|
INTERVALO
|
VÍA
|
DURACIÓN
|
|
GIARDIA LAMBLIA
|
Metronidazol
|
15
mg/kg/día
|
8
h
|
VO
|
7
días
|
|
Tinidazol1
|
50-60
mg/kg/día
|
24
h
|
VO
|
1
día
|
|
|
Paromomicina
|
25-35
mg/kg/día
|
8
h
|
VO
|
7-10
días
|
|
|
Mepacrina2
|
7
mg/kg/día (máx.: 300 mg)
|
8
h
|
VO
|
5-7
días
|
|
|
ENTAMOEBA
HISTOLYTICA
(portador
asintomático)
|
Paromomicina
|
25-35
mg/kg/día
|
8
h
|
VO
|
7-10
días
|
|
Iodoquinol2
|
30-40
mg/kg/día
|
8
h
|
VO
|
20
días
|
|
|
ENTAMOEBA
HISTOLYTICA
(colitis
amebiana)3
|
Metronidazol
|
30-50
mg/kg/día
|
8 h
|
VO
|
10
días
|
|
(o
tinidazol1) +
|
50-60
mg/kg/día
|
24 h
|
VO
|
3
días
|
|
|
Paromomicina
|
25-35
mg/kg/día
|
8 h
|
VO
|
10
días
|
|
|
(o
Iodoquinol2)
|
30-40
mg/kg/día
|
8 h
|
VO
|
20
días
|
|
|
ENTAMOEBA
HISTOLYTICA
(absceso
hepático)3
|
Metronidazol
|
30-50
mg/kg/día
|
8 h
|
VO
|
10
días
|
|
(o
tinidazol1) +
|
50-60
mg/kg/día
|
8 h
|
IV
|
10 días
|
|
|
Paromomicina
|
25-35
mg/kg/día
|
8 h
|
VO
|
10
días
|
|
|
(o
Iodoquinol2)
|
30-40
mg/kg/día
|
8 h
|
VO
|
20
días
|
|
|
CRYPTOSPORIDIUM
(inmuno-deprimido)
|
Paromomicina
|
25-35
mg/kg/día
|
8 h
|
VO
|
10 días
|
|
Claritromicina
|
15
mg/kg/día
|
12
h
|
VO
|
10
días
|
|
|
ENTEROBIUS
VERMICULARIS
|
Pamoato
de pyrantel
|
11
mg/kg/día
(max. 1g)
|
|
VO
|
Dosis Unica
Repetir en 2
Semanas
|
|
Mabendazol4
|
100 mg
|
12 h
|
VO
|
3 dias
|
|
|
TRICHURIS
TRICHIURA
|
Mebendazol4
|
100mg
|
12 h
|
VO
|
3 días
|
|
500mg/dosis
|
|
VO
|
1 día
|
||
|
Albendazol5
|
400
mg/dosis
|
|
VO
|
1
día
|
|
|
ASCARIS
LUMBRICOIDES
|
Mebendazol4
|
100mg
|
12 h
|
VO
|
3 días
|
|
500mg/dosis
|
|
VO
|
1 día
|
||
|
Pamoato
de pyrantel
|
11
mg/kg/día
(max. 1g)
|
24 h
|
VO
|
1 a 3 dias
|
|
|
ANCYLOSTOMA DUODENALE Y
NECATOR AMERICANUS
|
Mebendazol4
|
100mg
|
12 h
|
VO
|
3 días
|
|
500mg/dosis
|
|
VO
|
1 día
|
||
|
Albendazol5
|
400
mg/dosis
|
24 h
|
VO
|
3 a 5 días
|
|
|
STRONGYLOIDES
STERCORALIS
|
Ivermectina2,6
|
0,2
mg/kg/día
|
24
h
|
VO
|
2
días
|
|
Albendazol5
|
200
mg/dosis
|
12
h
|
VO
|
3-5
días.
7
días si
Hiper-infestación
|
|
|
HYMENOLEPIS
NANA
|
Prazicuantel2
(en
> 3 años)
|
25
mg/kg/día
|
24
h
|
VO
|
1
día y repetir
a
la semana
|
|
Niclosamida2
(en
< 3 años)
|
40
mg/kg/día la 1ª dosis y
20
mg/kg/día
las
siguientes
|
24h
|
VO
|
7
días y repetir ciclo a la semana
|
|
|
TAENIA
SOLIUM Y TAENIA SAGINATA
|
Prazicuantel2
|
5-10
mg/kg/día
|
24 h
|
VO
|
1 día
|
|
Niclosamida2
|
50
mg/kg/día
|
24 h
|
VO
|
1 día
|
|
|
TAENIA SOLIUM
(CISTICERCOSIS)7
|
Albendazol5
|
15
mg/kg/día (máx.: 800 mg)
|
12
h
|
VO
|
14-28
días
|
|
Prazicuantel2
|
50
mg/kg/día
|
8
h
|
VO
|
15
días
|
|
|
1 Tinidazol:
antiprotozoario oral aprobado por la OMS para
tratamiento de giardiasis, amebiasis intestinal y abceso hepático amebiano en
niños > 3 años (máx.: 2 g/día).
2 Se
debe asegurar que su principio activo sea unico.
3 Siempre
se tienen que tratar con dos fármacos. Paromomicina o Iodoquinol se
administran posteriomente a Metronidazol o Tinidazol. Contraindicado el uso de
corticoides.
4 Mebendazol: la monodosis de 100 mg/12 h está aprobada en > 2
años.
5 Albendazol:
la monodosis de éste fármaco a 400 mg está aprobada en niños > 4
años, pero es ampliamente usada para helmintiasis intestinales a cualquier edad.
Cuando se necesita un efecto tisular Albendazol debe administrarse en dos dosis diarias,
si la acción requerida es solo luminar se administra en una sola dosis.
6 Ivermectina:
la monodosis de este fármaco está aprobada para > 2-4 años.
7 Añadir
corticoides en cisticercosis si encefalitis, HTC o
convulsiones.
|
|||||